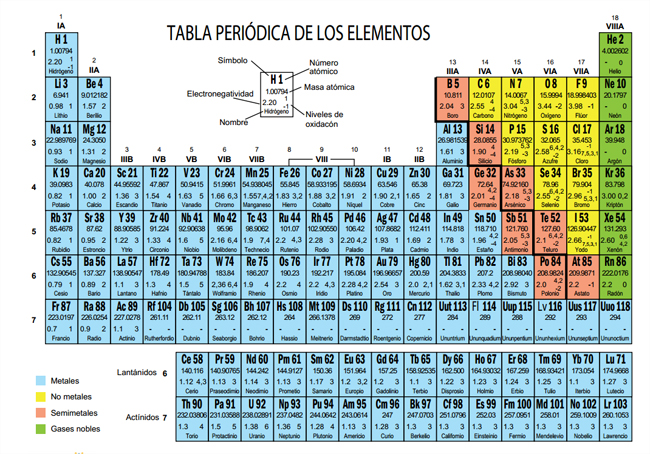
La electronegatividad es la capacidad que tiene un átomo para atraer electrones cuando forma enlace químico en una molécula. Así es como la definió el investigador estadounidense Linus Pauling (1901-1994), cuya escala de medición es aún hoy en día dogma de fe. ¿Sabes cuál es el elemento más electronegativo?
El elemento con mayor electronegatividad de la tabla periódica es el fluor, con un valor en la citada escala de Pauling de 3.98. Tras él se sitúan el oxígeno (3,44), el cloro (3,16) y el nitrógeno (3.04), siendo el francio el elemento con menor capacidad para atraer los electrones de lo átomos vecinos (0.7).
El fluor no solo es el elemento más electronegativo, sino también el más reactivo, siendo capaz de crear compuestos con casi todos los demás elementos. Su número atómico es el 9, su símbolo F y está localizado en el grupo 17, el que ocupan los halógenos.
Es importante explicar que la electronegatividad de un elemento depende de su estado de valencia, por lo que no es una propiedad atómica invariable, sino que depende del «entorno» de un mismo átomo en distintos enlaces de distintas moléculas.
Para más información, puedes descargarte aquí la tabla periódica de elementos.
Flúor
El elemento de mayor energía de ionizacion es el helio, y de menor el Cesio.La unidad de energía de iozanizacion es el electrón voltio
estas cascao
estas cascao
Esa tabla no me sirve para nada, no tiene los valores bien dados.
Es incorrecto, el flúor es el mayor (4.0), por lo que esta tabla dice que tiene 3.98, aunque no se crea, los números cuentan.
El fluor.
Cual.de estos elementos es el.q.posee mayor eletctronegatividad p ge h as
Mejor aprende a escribir
hola
biennnnnnn
biennnnnnnnnnnnnnnnnnnnnnnnnn
oye cabezon estas mamao